Ikatan Logam: Pengertian, Ciri, Sifat dan Proses Pembentukan Beserta Contoh Lengkapnya
Tahukah anda apa yang dimaksud dengan ikatan logam??? Jika Anda belum mengetahuinya, Anda tepat untuk mengunjungi guruducacy.com. Karena pada kesempatan kali ini kita akan membahas pengertian ikatan logam, ciri-ciri ikatan logam, sifat ikatan logam, proses terbentuknya ikatan logam, dan contoh lengkapnya. Oleh karena itu, mari kita simak ulasan di bawah ini.
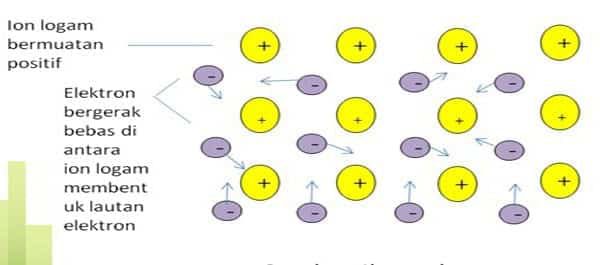
Pengertian ikatan logam
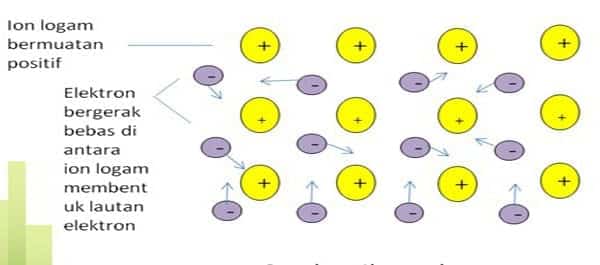
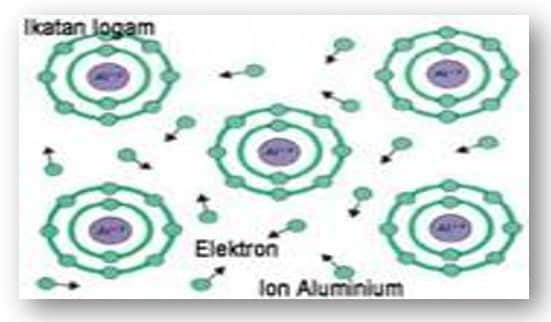
Ikatan logam adalah ikatan kimia yang dibentuk oleh pembagian elektron valensi antara atom logam. Contoh: logam besi, seng, dan perak. Ikatan logam bukanlah ikatan ionik atau ikatan kovalen. Salah satu teori yang diajukan untuk menjelaskan ikatan logam adalah teori lautan elektron. Contoh ikatan logam Posisi elektron valensi atom besi (Fe) dapat tumpang tindih dengan posisi elektron valensi atom Fe lainnya.
Tumpang tindih antara elektron valensi ini memungkinkan elektron valensi setiap atom Fe bergerak bebas di ruang antara ion Fe+ untuk membentuk lautan elektron. Karena muatannya berlawanan (Fe2+ dan 2 e–), gaya tarik menarik terjadi antara ion Fe+ dan elektron bebas ini. Akibatnya, apa yang disebut ikatan terbentuk ikatan logam.
Sifat ikatan logam
- Atom logam dapat dibandingkan dengan bola pingpong yang padat.
- Atom logam memiliki sedikit elektron valensi, sehingga sangat mudah kehilangannya dan membentuk ion positif.
- Oleh karena itu, kulit terluar atom logam relatif longgar (banyak tempat kosong) sehingga elektron dapat berpindah dari satu atom ke atom lainnya.
- Mobilitas elektron pada logam sangat bebas sehingga elektron valensi pada logam mengalami delokalisasi, yaitu keadaan dimana elektron valensi tidak berada pada posisi tetap dalam satu atom, tetapi terus berpindah dari satu atom ke atom lainnya.
- Elektron valensi bercampur membentuk awan elektron yang mengelilingi ion logam positif.
Adanya ikatan logam menyebabkan logam menjadi:
Logam berwujud padat pada suhu dan tekanan standar, kecuali unsur merkuri dan galium yang keduanya berwujud cair. Sebagai pengingat, sifat-sifat logam adalah sebagai berikut:
- Memiliki konduktivitas termal dan listrik yang tinggi.
- Bersinar dan memantulkan cahaya.
- Dapat difalsifikasi.
- Memiliki berbagai kekuatan mekanik.
Harus diingat bahwa ikatan logam adalah gaya utama yang menyatukan atom-atom logam. Ikatan logam adalah hasil tarikan muatan positif logam dan muatan negatif elektron yang bergerak bebas.
Sifat logam tidak dapat dimasukkan dalam kriteria ikatan seperti ikatan kovalen atau ikatan ionik. Senyawa ionik tidak dapat menghantarkan listrik dalam fase padat, dan senyawa ionik bersifat rapuh (berlawanan dengan logam). Dan; Atom senyawa logam hanya mengandung satu sampai tiga elektron valensi. Oleh karena itu atom-atom ini tidak dapat membentuk ikatan kovalen. Senyawa kovalen adalah konduktor listrik yang buruk dan umumnya berbentuk cair (dengan sifat berlawanan membentuk logam). Oleh karena itu, logam membentuk model ikatan yang berbeda.
Proses pembentukan ikatan logam
Dalam ikatan logam terjadi proses saling meminjamkan elektron, hanya saja jumlah atom yang bersama-sama meminjamkan elektron valensinya (elektron pada kulit terluar) tidak hanya antara dua, melainkan beberapa atom, tetapi dalam jumlah yang tidak terbatas. Setiap atom melepaskan elektron valensi untuk digunakan bersama, sehingga akan terjadi ikatan yang menarik antara atom-atom yang berdekatan.
Jarak antara atom-atom tersebut akan tetap sama, artinya jika suatu atom bergerak menjauh maka gaya tarik-menarik akan menariknya kembali ke posisi semula dan jika bergerak terlalu dekat akan timbul gaya tolak karena jarak inti atom terlalu dekat. satu sama lain muatan listriknya sama sehingga posisi atom akan tetap relatif terhadap atom lainnya.
Dalam ikatan logam, inti atom berjarak pada jarak tertentu dan tersusun secara teratur, sedangkan elektron dibagi seolah-olah membentuk awan elektron. Dalam logam, orbital atom terluar yang diisi dengan elektron bergabung menjadi sistem terdelokalisasi yang menjadi dasar pembentukan ikatan logam. Delokalisasi adalah keadaan dimana elektron valensi tidak memiliki posisi yang tetap dalam satu atom, tetapi selalu berpindah dari satu atom ke atom lainnya.
Atom logam dapat berikatan bersama ke segala arah untuk membentuk molekul yang sangat besar. Satu atom akan berikatan dengan beberapa atom lain di sekitarnya. Akibatnya, atom-atom ini terikat erat dan logam padat (kecuali Hg) dan umumnya keras.
Contoh ikatan logam:
Perbandingan sifat fisika senyawa logam dengan senyawa non logam
| Logam | Bukan metal | ||
| 1. | Padatan logam adalah konduktor listrik yang baik | 1. | Padatan non-logam umumnya tidak menghantarkan listrik |
| 2. | Memiliki kilau metalik | 2. | Tidak mengkilap |
| 3. | Kuat dan keras (bila digunakan sebagai paduan) | 3. | Sebagian besar non-logam tidak kuat dan mudah dibentuk |
| 4. | Bisa ditekuk dan diregangkan | 4. | Biasanya rapuh dan pecah saat ditekuk atau diregangkan |
| 5. | konduktor panas yang baik | 5. | Sulit menghantarkan panas |
| 6. | Sebagian besar logam memiliki kerapatan tinggi | 6. | Sebagian besar non-logam memiliki kerapatan rendah |
| 7. | Sebagian besar logam memiliki titik didih dan titik leleh yang tinggi | 7. | Sebagian besar non-logam memiliki titik didih dan titik leleh yang rendah |
REAKSI SENYAWA LOGAM:
Logam alkali memiliki beberapa sifat fisik, antara lain semuanya lunak, putih mengkilat, dan mudah dipotong. Jika logam ini dibiarkan di udara terbuka, permukaannya akan kusam karena logam ini mudah bereaksi dengan air atau oksigen, dan biasanya tersimpan dalam minyak tanah.
Dengan meningkatnya nomor atom, begitu pula tingkat kelembutannya. Tingkat pelunakan logam alkali meningkat tergantung pada peningkatan nomor atom logam. Sifat kimia logam alkali tanah dapat diamati antara lain dari reaksinya terhadap air. Reaksinya dengan air menghasilkan gas hidrogen dan hidroksida dan cukup panas. Reaktivitas untuk air dingin meningkat dengan meningkatnya jumlah logam.
Logam alkali tanah, kecuali berilium, semuanya berwarna putih, mudah dipotong dan tampak lebih cerah saat dipotong, dan cepat kusam di udara. Reaktivitas terhadap air bervariasi. Berilium dapat bereaksi dengan air dalam keadaan bercahaya dan air tersebut berbentuk uap. Magnesium bereaksi lambat dengan air dingin dan lebih cepat saat menjadi lebih hangat, logam alkali tanah lainnya bereaksi sangat cepat dengan air dingin menghasilkan gas hidrogen dan hidroksida dan menghasilkan banyak panas.
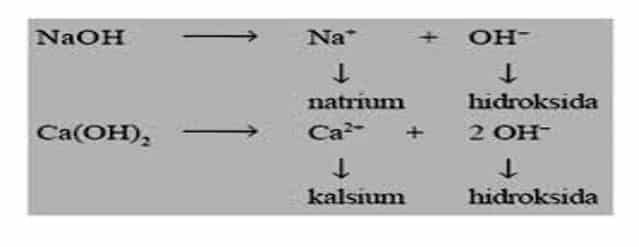
Senyawa klorida dari logam alkali dan alkali tanah larut dalam air untuk membentuk ion hidrasi sederhana. banyak klorida kovalen atau sedikit kovalen menjalani hidrolisis untuk menghasilkan klorida dan oksida atau hidroksilnya. Misalnya, larutan aluminium klorida bereaksi dengan air membentuk aluminium hidroksida.
Demikianlah apa yang dimaksud dengan ulasan Ikatan Logam: Pengertian, Ciri, Sifat dan Proses Pembentukan Beserta Contoh Lengkapnya Semoga apa yang telah diulas di atas bermanfaat bagi para pembaca. Demikian dan terima kasih.
Baca juga artikel referensi terkait lainnya disini:
- Ikatan Kovalen: Pengertian, Jenis dan Proses Pembentukannya Beserta Contoh Lengkapnya.
- Termokimia: Pengertian Lengkap, Sistem, Reaksi, Rumus dan Contohnya
- √ Kertas ikatan kimia: definisi, jenis dan gambar lengkap
- Ikatan ion: pengertian, ciri dan penentuan terjadinya, serta contoh lengkapnya
Posting Ikatan Logam: Pengertian, Ciri, Sifat dan Proses Pembentukan serta Contoh Lengkapnya muncul pertama kali di GuruPendidikan.Com.
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa