Southhydrolysis: definisi, jenis dan formula, beserta contoh lengkapnya – Apakah Anda tahu apa yang dimaksud? Southhydrolysis ??? Kalau belum tahu, kamu berkunjung ke guruducacy.com kan.
Karena pada kesempatan kali ini kita akan mengulas secara lengkap pengertian hidrolisis garam, jenis hidrolisis garam dan rumus hidrolisis garam beserta contoh soalnya. Oleh karena itu, mari kita simak ulasan di bawah ini.
Baca juga artikel terkait: Hukum Archimedes: Pengertian, Bunyi, Rumus dan Contoh Soal Lengkap

Definisi hidrolisis garam
Southhydrolysis adalahmemecah garam dalam air untuk menghasilkan asam dan basa.“
Bagaimana hidrolisis terjadi?
Hidrolisis suatu garam hanya terjadi JIKA salah satu atau kedua komponen penyusun garam tersebut merupakan asam lemah dan/atau basa lemah. Jika komponen garamnya adalah asam kuat dan basa kuat, komponen ionik dari asam kuat atau basa kuat tidak akan terhidrolisis.
Baca juga artikel terkait: Laju Reaksi: Pengertian, Faktor-faktor yang Mempengaruhi, dan rumus lengkap serta contoh soal
Berdasarkan penjelasan tersebut, kation dan anion yang dapat mengalami reaksi hidrolisis adalah kation dan anion garam yang merupakan elektrolit lemah. Sedangkan kation garam dan anion yang merupakan elektrolit kuat tidak terhidrolisis.
Reaksi garam dengan air, dimana komponen garam (kation atau anion) yang berasal dari asam lemah atau basa lemah bereaksi dengan air membentuk ion H3Oh+(=H+) atau ion OH–.
Jika hidrolisis H3Oh+ maka larutan bersifat asam, tetapi jika dihidrolisis menghasilkan ion OH– maka larutan bersifat basa.
Baca juga artikel terkait: Larutan Elektrolit: Pengertian, Ciri-Ciri, dan Jenisnya Lengkap Beserta Contohnya
SIFAT LARUTAN BERBASIS ASAM
Pencampuran larutan asam dengan larutan basa akan menghasilkan garam dan air. Reaksi asam dengan basa membentuk garam disebut reaksi netralisasi. Namun, garam bisa bersifat asam, basa atau netral.
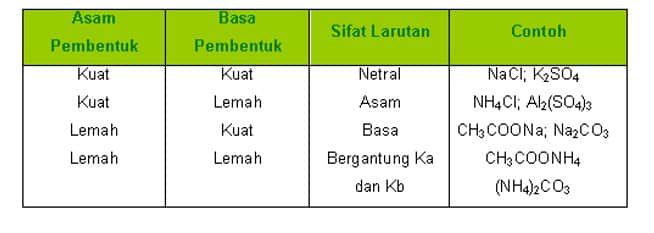
Sifat-sifat garam bergantung pada jenis asam dan komponen dasarnya. Garam dapat dibentuk dari asam kuat dan basa kuat, asam lemah dan basa kuat, asam kuat dan basa lemah, atau asam lemah dan basa lemah.
Dengan demikian, sifat asam-basa suatu garam dapat ditentukan dari kekuatan asam dan basa penyusunnya. Keasaman atau kebasaan garam ini disebabkan oleh sebagian garam terlarut bereaksi dengan air. Proses melarutkan sebagian garam, bereaksi dengan air, disebut hidrolisis (hidro artinya air dan lisis artinya penguraian).

Baca juga artikel terkait: Solusi buffer: Definisi lengkap, fungsi dan jenis beserta contohnya
JENIS-JENIS GARAM HIDROLISASI
Garam terdiri dari empat jenis, yang terbagi berdasarkan komponen asam-basa penyusunnya.




Baca juga artikel terkait: Larutan garam: Definisi lengkap, ciri-ciri dan sifat-sifat beserta contohnya
Jenis hidrolisis garam
Jika dilihat dari komponen pembentuk garam dan dapat tidaknya garam terurai bila direaksikan dengan air, maka reaksi hidrolisis dapat dibedakan sebagai berikut.
1. Hidrolisis parsial
Hidrolisis parsial adalah ketika garam direaksikan dengan air hanya satu / beberapa ion yang mengalami reaksi hidrolisis, sedangkan yang lainnya tidak. Komponen penyusun garam yang mengalami reaksi hidrolisis parsial ini adalah asam lemah dan basa kuat atau sebaliknya.
2. Total hidrolisis
Hidrolisis total adalah reaksi penguraian semua garam oleh air, dimana komponen garamnya terdiri dari asam lemah dan basa lemah.
Berdasarkan jenis ion yang dihasilkan ketika garam dilarutkan dalam air, proses hidrolisis dapat dibagi menjadi beberapa jenis berikut.
Baca juga artikel terkait: Larutan Alkaline: Pengertian, Ciri dan Sifat Lengkap Beserta Contohnya
3. Hidrolisis anion
Jika garam yang terdiri dari komponen molekul asam lemah dan basa kuat direaksikan dengan molekul air, garam ini hanya akan terhidrolisis sebagian dalam air dan akan menghasilkan ion basa (OH-). Dengan kata lain, anion asam lemah dihidrolisis, sedangkan kation basa kuat tidak.
Contoh:
CH3COONa(aq) → CH3COO–(aq) + Na+ (aq)
CH3COO– + H2O ↔ CH3COOH + OH–
Na+ + H2O → tidak terjadi reaksi
Dari contoh di atas dijelaskan bahwa CH3COO– yang bertindak sebagai anion asam lemah dihidrolisis menjadi OH ketika direaksikan dengan molekul air (H2O) sedangkan Na+ yang bertindak sebagai kation basa kuat tidak dihidrolisis ketika direaksikan dengan molekul air.
Terakhir, garam dengan komponen pembentuk asam lemah dan basa kuat, bila direaksikan dengan air, akan terhidrolisis sebagian dan menghasilkan ion yang bersifat basa.
Baca juga artikel terkait: Larutan asam: Pengertian lengkap, ciri-ciri dan sifat-sifat beserta contohnya
4. Hidrolisis kation
Mirip dengan reaksi hidrolisis antara garam dengan komponen molekul asam lemah dan basa kuat yang bereaksi dengan molekul air, jika garam dengan komponen asam kuat dan basa lemah dilarutkan dalam molekul air, ia juga akan mengalami hidrolisis parsial dan menghasilkan ion yang bersifat asam ( H+). Hal ini terjadi karena hanya kation basa lemah yang terhidrolisis, sedangkan anion asam kuat tidak mengalami hidrolisis.
Contoh:
NH4Cl → NH4+ + Cl–
NH4+ + H2O ↔ NH4OH + H+
Cl– + H2O → tidak terjadi reaksi
Berdasarkan contoh di atas dapat dijelaskan bahwa NH4+ yang berperan sebagai basa lemah terhidrolisis menghasilkan ion yang bersifat asam yaitu H+. Sedangkan Cl- yang merupakan anion asam kuat tidak terhidrolisis.
Baca juga artikel terkait: Getaran Harmonik: Pengertian, Istilah dan Rumus Beserta Contoh Soal Lengkap
5. Kation dan anion terhidrolisis
Jika suatu garam dengan komponen asam lemah dan basa lemah direaksikan dengan molekul air, maka akan mengalami hidrolisis total. Hal ini dapat terjadi karena kation basa lemah dan anion asam lemah dapat terhidrolisis sempurna. Reaksi hidrolisis ini menghasilkan ion H+ atau OH-.
Contoh:
CH3COONH4 → CH3COO– + NH4+
CH3COO– + H2O ↔ CH3COOH + OH–
NH4+ + H2O ↔ NH4OH + H+
Contoh di atas menjelaskan bahwa dua komponen penyusun garam CH3COO- (anion dari asam lemah) dan NH4+ (kation dari basa lemah) dapat terhidrolisis sempurna, masing-masing menghasilkan ion basa (OH-) dan ion asam (H+ ) menghasilkan ). ).
Contoh soal hidrolisis garam
1. Konsentrasi NH4Cl adalah 0,4 M, dengan kb NH3 = 10-5
Menjawab:

hidrolisis 1
2. pH 0,4 M NH4Cl adalah (kb NH3 = 10-5)
menjawab:

Berikut ini adalah beberapa contoh bersama dengan solusi untuk pertanyaan terkait hidrolisis garam Apa yang baru saja kita pelajari bersama:
- Berapa pH larutan 100 ml larutan natrium sianida 0,01 M? (KA HCN = 10-10)
Resolusi:
Larutan natrium sianida terbentuk dari campuran basa kuat (NaOH) dan asam lemah (HCN). Oleh karena itu, larutan garam mengalami hidrolisis parsial dan bersifat basa.
NaCN(SAYA) → Setelah+(SAYA) +CN–(SAYA)
Ion yang terhidrolisis adalah ion CN–. konsentrasi ion CN– adalah 0,01 M. Oleh karena itu, pH larutan garam dapat diperoleh dengan persamaan berikut:
[OH–] = {(Kw /kA)([ion yang terhidrolisis])}1/2
[OH–] = {(10-14 / 10-10)(0,01)}1/2
[OH–] = 10-3 M
Jadi, pOH larutannya adalah 3. Jadi, pH larutan garamnya adalah 11.
- Berapa pH larutan 200 ml larutan barium asetat 0,1 M? (KA CH3COOH = 2.10-5)
Resolusi:
Larutan barium asetat terbentuk dari campuran basa kuat (Ba(OH))2) dengan asam lemah (CH3COOH). Oleh karena itu, larutan garam mengalami hidrolisis parsial dan bersifat basa.
Ba(CH3MENDEKUT)2(aq) → Ba+2(SAYA) + 2CH3MENDEKUT–(SAYA)
Ion yang terhidrolisis adalah ion CH3MENDEKUT–. konsentrasi ion CH3MENDEKUT– adalah 0,2 M. Oleh karena itu, pH larutan garam dapat diperoleh dengan persamaan berikut:
[OH–] = {(Kw /kA)([ion yang terhidrolisis])}1/2
[OH–] = {(10-14 / 2.10-5)(0,2)}1/2
[OH–] = 10-5 M
Jadi, pOH larutannya adalah 5. Jadi, pH larutan garamnya adalah 9.
- Hitung pH larutan NH4Cl 0,42M! (KB NH4OH = 1.8.10-5)
Resolusi:
Larutan amonium klorida terbentuk dari campuran basa lemah (NH4OH) dengan asam kuat (HCl). Oleh karena itu, larutan garam mengalami hidrolisis parsial dan bersifat asam.
NH4kl(SAYA) → NH4+(SAYA) + Kl–(SAYA)
Ion yang terhidrolisis adalah ion NH4+. konsentrasi ion NH4+ adalah 0,42 M. Oleh karena itu, pH larutan garam dapat diperoleh dengan persamaan berikut:
[H+] = {(Kw /kB)([ion yang terhidrolisis])}1/2
[H+] = {(10-14 /1,8.10-5)(0,42)}1/2
[H+] = 1.53.10-5 M
Oleh karena itu, pH larutan garam adalah 4,82.
- Hitung pH larutan NH4CN2.00M! (KA HCN = 4.9.10-10 dan KB NH4OH = 1.8.10-5)
Resolusi:
Larutan amonium sianida terbentuk dari basa lemah (NH4OH) dengan asam lemah (HCN). Larutan garam dengan demikian mengalami hidrolisis sempurna.
NH4kl(SAYA) → NH4+(SAYA) +CN–(SAYA)
Ion yang terhidrolisis adalah ion NH4+ dan ion CN–. Oleh karena itu, pH larutan garam dapat diperoleh dengan persamaan berikut:
[H+] = {Kw (KA/kB)}1/2
[H+] = {10-14 (4,9.10-10 /1,8.10-5)}1/2
[H+] = 5,22,10-10 M
Oleh karena itu, pH larutan garam adalah 9,28.
- Berapa massa garam NaCN yang harus dilarutkan untuk membentuk 250 ml larutan dengan pH 10? (KA HCN = 10-10 dan tuan NaCN = 49)
Resolusi:
Larutan natrium sianida terbentuk dari campuran basa kuat (NaOH) dan asam lemah (HCN). Oleh karena itu, larutan garam mengalami hidrolisis parsial dan bersifat basa.
NaCN(SAYA) → Setelah+(SAYA) +CN–(SAYA)
pH = 10, berarti pOH = 4
Karena itu, [OH–] = 10-4 M
Perhitungan pH larutan garam dapat diperoleh dengan persamaan berikut:
[OH–] = {(Kw/kA)([ion yang terhidrolisis])}1/2
10-4 = {(10-14 / 10-10)[ion yang terhidrolisis]}1/2
[ion yang terhidrolisis] = 10-4 M
Konsentrasi garam NaCN yang dibutuhkan adalah 10-4 M. Volume larutannya adalah 250 mL = 0,25 L. Oleh karena itu, mol garam NaCN yang diperlukan adalah:
Mol = Volume x molar
Mol = 0,25 x 10-4 = 2,5 x 10-5 tikus tanah
Jadi, massa garam NaCN yang dibutuhkan adalah 2,5 x 10-5 x 49 = 1,225 x 10-3 gram = 1,225 mg.
Ini ulasan lengkapnya. Semoga apa yang telah diulas di atas bermanfaat bagi para pembaca. Demikian dan terima kasih.
BIBLIOGRAFI
Tua, Michael. 2007. KIMIA 2 Untuk SMA Kelas XI. Jakarta: Penerbit Erlangga
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa