Memahami asam dan basa
Asam dan basa merupakan bahan kimia yang banyak digunakan dalam kehidupan sehari-hari.
-
Asam
Istilah acid (asam) berasal dari bahasa latin “Acetum” yang berarti cuka, karena diketahui bahwa zat utama dalam cuka adalah asam asetat. Secara umum, asam adalah zat yang rasanya asam.
-
Basis
Basa (alkali) berasal dari bahasa Arab yang berarti abu. Pada umumnya basa adalah zat yang berasa pahit dan bersifat kaustik.
Teori asam Svante Arrhenius
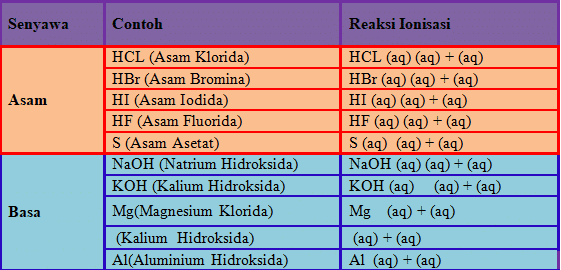
Arrhenius mengatakan bahwa molekul elektrolit selalu menghasilkan ion positif dan negatif ketika dilarutkan dalam air. Pada tahun 1984, ilmuwan Swedia Svante Arrhenius mendefinisikan asam berdasarkan reaksi ionisasi. Menurut Arrhenius, asam adalah zat yang bila dilarutkan dalam air akan menghasilkan ion. Basa adalah zat yang, ketika dilarutkan dalam air, menghasilkan ion.
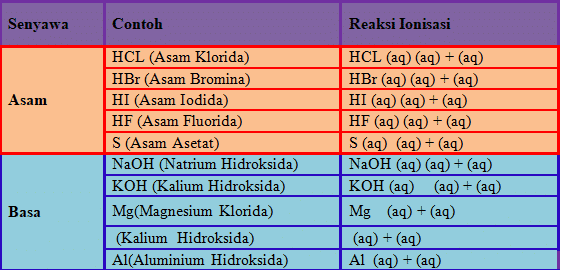
untuk asam di mana setiap molekul dapat menghasilkan lebih dari satu ion yang dikelompokkan asam poliprotik.
Contoh:
Asam sulfat dalam air
S(aq) (aq) + (aq)
(aq) (aq) + (aq)
Molekul asam ini dapat menghasilkan 2 ion. Oleh karena itu, asam sulfat diklasifikasikan sebagai asam diprotik.
Asam fosfat dalam air
P(aq) (aq) + (aq)
(aq) (aq) + (aq)
(aq) (aq) + (aq)
Satu molekul asam ini dapat menghasilkan 3 ion. Oleh karena itu, asam fosfat diklasifikasikan sebagai asam triprotik.
Teori asam dan basa Bronsted-Lowry
Pada tahun 1923, ilmuwan Denmark Johannes Bronsted dan ilmuwan Inggris Thomas Lowry mengusulkan teori asam dan basah berdasarkan transfer proton.
Teori
- Asam adalah donor proton (ion hidrogen).
- Basa adalah akseptor proton (ion hidrogen).
Definisi asam basa yang dikemukakan oleh Bronsted-Lowry mengoreksi kelemahan teori asam basa Arrhenius. Definisi asam basa Arrhenius hanya berlaku untuk senyawa yang larut dalam pelarut berair karena reaksi ionisasi yang menghasilkan ion dan ion hanya terjadi dalam pelarut berair.
Dalam persamaan reaksi asam-basa berdasarkan teori Bronsted-Lowry, asam dan basa masing-masing memiliki pasangan. Pasangan asam disebut basa konjugasi sedangkan pasangan basa disebut asam konjugasi.
Ada beberapa hal yang perlu diperhatikan dalam asam basa konjugasi:
- Molekul atau ion yang membentuk pasangan asam-basa harus berbeda satu ion saja. Dalam pasangan, asam selalu memiliki ion yang melebihi basa.
- Asam konjugat dapat ditemukan dengan menambahkan satu ion ke dalam zat, sedangkan basa konjugat dapat ditemukan dengan menghilangkan satu ion dari zat tersebut.
- Molekul atau ion yang mengandung atom H dan atom yang memiliki pasangan elektron bebas dapat bersifat asam (pemberi ion) dan basa (menerima ion 0). Zat seperti itu disebut amfibrotik atau amfoter.
Kelebihan asam – basa menurut Bronsted – Lowry :
- Konsep asam-basa menurut Bronsted-Lowry tidak terbatas pada pelarut air, tetapi juga menggambarkan reaksi asam-basa dalam pelarut lain atau bahkan reaksi tanpa pelarut.
- Asam dan basa Bronsted–Lowry bukan hanya molekul, tetapi juga bisa berupa kation atau anion. Konsep asam dan basa Bronsted-Lowry dapat menjelaskan sifat asam suatu senyawa.
Kekuatan asam dan basa
Senyawa asam basa dapat dikelompokkan berdasarkan kekuatannya, yaitu:
Asam atau basa yang terdisosiasi sebagian atau seluruhnya menjadi ion-ionnya adalah asam kuat atau basa kuat
Contoh:
- Asam klorida (HCL) adalah asam kuat yang mengionisasi sepenuhnya menjadi dan ion.
HCL(aq) (aq) + (aq)
- Asam lemah dan basa lemah
Jika hanya sebagian kecil dari asam atau basa yang terurai menjadi ion-ionnya, maka itu adalah asam lemah atau basa lemah.
Identifikasi asam – basa
Senyawa asam dapat dibedakan dengan senyawa basa, salah satunya dengan cara mencicipi rasanya. Namun, tidak semua zat dapat diidentifikasi dengan cara ini. Senyawa asam-basa dapat diidentifikasi dengan aman menggunakan indikator. Indikator adalah zat warna yang berbeda warnanya ketika dalam kondisi asam dan basa. Indikator yang dapat digunakan adalah kertas lakmus, indikator asam basa dan indikator alam.
-
Identifikasi asam – basa dengan kertas lakmus
Senyawa basa sam dapat diidentifikasi menggunakan kertas lakmus dengan mengamati perubahan warna kertas lakmus ketika bereaksi dengan larutan. Ada dua jenis kertas lakmus, yaitu kertas lakmus merah dan kertas lakmus biru.
Ketika dicelupkan ke dalam larutan asam dan larutan basa, kertas lakmus merah dan kertas lakmus biru akan menimbulkan perubahan warna yang berbeda. Larutan asam adalah jus lemon dan larutan cuka, sedangkan larutan basa adalah air sabun dan larutan soda kue.
Kertas lakmus merah yang dicelupkan ke dalam larutan asam tidak akan berubah warna, jika kertas dicelupkan ke dalam larutan basa akan berubah warna menjadi biru. Sebaliknya, jika kertas lakmus biru dicelupkan ke dalam larutan asam, maka lakmus tersebut akan berubah menjadi merah. Sedangkan jika dicelupkan ke dalam larutan basa, warnanya tetap biru.
-
Mengidentifikasi asam – basa dengan indikator asam – basa
Selain kertas lakmus, kita juga bisa menggunakan indikator asam basa untuk membedakan asam dan basa. Indikator asam-basa adalah zat kimia yang memiliki warna berbeda dalam larutan asam dan basa. Sifat ini menyebabkan indikator asam-basa digunakan untuk mengidentifikasi sifat asam dan basa. Ada beberapa jenis indikator asam-basa, antara lain fenolftalein, jingga metil, biru bromotimil, ungu metil, ungu bromokresol, merah fenol, timolftalein, dan jingga metil.
Demikian artikel Duniadunia.co.id mengenai Teori Asam Basa: Svante Arrhenius, Bronsted-Lowry, Kekuatan, Contoh, Identifikasi, Pengertian, semoga artikel ini bermanfaat untuk sobat semua.
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa