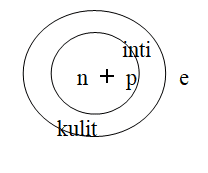
Partikel atom dasar
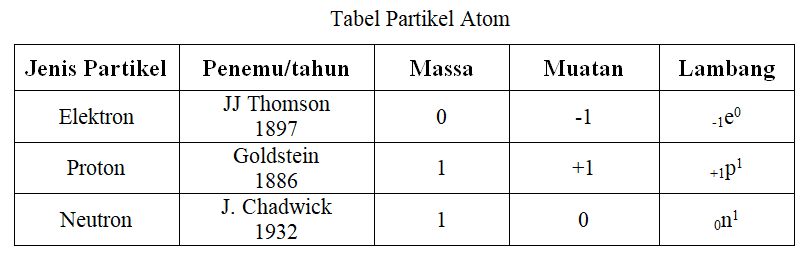
Partikel dasar penyusun atom adalah proton, neutron, dan elektron. Inti atom terdiri dari proton dan neutron yang dikelilingi oleh elektron yang terletak di kulit atom. Atom bersifat netral, artinya jumlah proton (muatan positif) sama dengan jumlah elektron (muatan negatif).
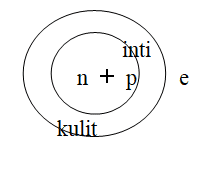
Susunan elektron dalam atom
Elektron yang selalu bergerak mengelilingi inti atom tampak berada pada tingkat energi tertentu yang dikenal sebagai kulit atom.
Konfigurasi elektron adalah susunan atau susunan elektron berdasarkan tingkat energinya dalam suatu atom. Tingkat energi yang paling dekat dengan inti atau tingkat energi pertama (n = 1) diberi lambang K atau disebut kulit K. Tingkat energi kedua diberi lambang L, tingkat energi ketiga M dan seterusnya.
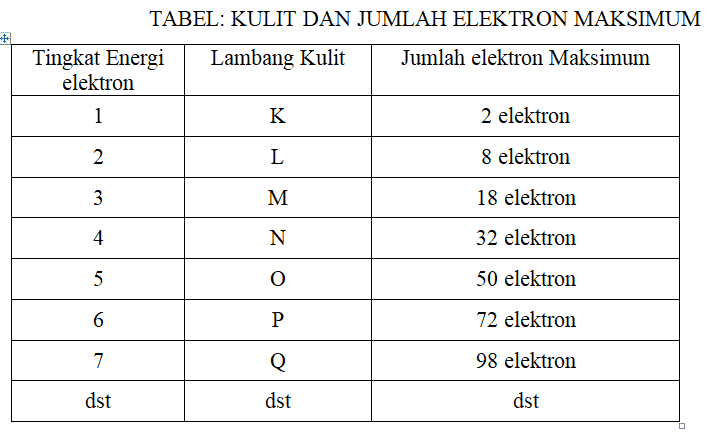
Jumlah maksimum elektron yang dapat menempati setiap tingkat energi sesuai dengan 2n2(akan dijelaskan lebih detail pada kelas 3), sehingga jumlah elektron pada setiap tingkat energi utama dapat dilihat pada tabel di bawah ini.
Pada tahun 1803, John Dalton mengutarakan pendapatnya tentang atom. Teori atom Dalton didasarkan pada dua hukum, yaitu hukum kekekalan massa (hukum Lavoisier) dan hukum komposisi zat padat (hukum Prouts). Lavosier mengatakan bahwa “massa total zat sebelum reaksi akan selalu sama dengan massa total hasil reaksi”. Sedangkan Prouts menyatakan bahwa “Perbandingan massa unsur-unsur dalam suatu senyawa selalu tetap”. Dari kedua hukum tersebut, Dalton mengemukakan pendapatnya tentang atom sebagai berikut:
- Atom adalah bagian terkecil dari materi yang tidak dapat dibagi lagi
- Atom digambarkan sebagai bola padat yang sangat kecil, suatu unsur memiliki atom yang identik dan berbeda untuk unsur yang berbeda
- Atom bergabung untuk membentuk senyawa dalam rasio bilangan sederhana dan bilangan bulat. Misalnya, air terdiri dari atom hidrogen dan atom oksigen
- Reaksi kimia adalah pemisahan atau kombinasi atau penataan ulang atom, sehingga atom tidak dapat diciptakan atau dihancurkan.
Kelemahan
Teori Dalton tidak menjelaskan hubungan antara pembubaran senyawa dan konduktivitas arus listrik.
Berdasarkan penemuan tabung katoda yang lebih baik oleh William CrookerJadi JJ Thomson penelitian lebih lanjut tentang sinar katoda dan dapat ditentukan bahwa sinar katoda adalah partikel, karena dapat memutar roda yang ditempatkan antara katoda dan anoda. Dari hasil percobaan tersebut, Thomson menyatakan bahwa sinar katoda merupakan partikel subatom yang bermuatan negatif dan disebut sebagai elektron.
Atom adalah partikel netral, karena elektron bermuatan negatif, maka harus ada partikel bermuatan positif lainnya untuk menetralkan muatan negatif elektron tersebut. Dari penemuan tersebut, Thomson mengoreksi kelemahan teori atom Dalton dan mempresentasikan teori atomnya yang dikenal dengan teori atom Thomson. Yang mengatakan bahwa:
“Atom adalah bola padat yang bermuatan positif dan elektron bermuatan negatif tersebar di dalamnya.”
Kelemahan
Kelemahan model atom Thomson tidak dapat menjelaskan susunan muatan positif dan negatif dalam bola atom.
Rutherford dengan dua muridnya (Hans Geiger dan Erners Masreden) melakukan percobaan yang dikenal sebagai hamburan sinar alfa (λ) pada lembaran tipis emas. Sebelumnya telah ditemukan adanya partikel alfa, yaitu partikel yang bermuatan positif dan bergerak dalam garis lurus, memiliki daya tembus yang besar sehingga mampu menembus lembaran kertas yang tipis.
Eksperimen tersebut sebenarnya bertujuan untuk menguji pendapat Thomson, yaitu apakah atom benar-benar merupakan bola padat positif yang bila dikenai partikel alfa akan dipantulkan atau dibelokkan. Dari pengamatan mereka diketahui bahwa ketika partikel alfa ditembakkan pada lempengan emas yang sangat tipis, sebagian besar partikel alfa lolos (terdapat deviasi sudut kurang dari 1°), namun dari pengamatan Marsden diperoleh fakta bahwa satu dari 20.000 partikel alfa akan semakin menyimpang pada sudut 90 °.
Berdasarkan gejala yang terjadi, diperoleh kesimpulan sebagai berikut:
- Atom bukanlah bola padat karena hampir semua partikel alfa dilewati
- Jika lempengan emas dianggap sebagai lapisan atom emas, maka di dalam atom emas terdapat banyak partikel kecil yang bermuatan positif.
- Partikel ini adalah partikel penyusun inti atom, berdasarkan fakta bahwa 1 dari 20.000 partikel alfa akan dibelokkan. Jika perbandingan 1:20.000 adalah perbandingan diameter, maka ukuran inti atom kira-kira 10.000 lebih kecil dari ukuran keseluruhan atom.
Berdasarkan fakta-fakta yang diperoleh dari percobaan tersebut, Rutherford mengusulkan model atom yang dikenal sebagai model atom Rutherford apa yang dinyatakan Atom terdiri dari inti bermuatan positif yang sangat kecil dikelilingi oleh elektron bermuatan negatif. Rutherford menduga bahwa di dalam inti atom terdapat partikel netral yang berfungsi mengikat partikel positif agar tidak saling tolak menolak.
Kelemahan:
Tidak dapat menjelaskan mengapa elektron tidak jatuh ke dalam inti atom
Pada tahun 1913, seorang fisikawan Denmark menelepon Neils Bohr Kekeliruan atom Rutherford dikoreksi oleh eksperimennya pada spektrum atom hidrogen. Eksperimen ini berhasil memberikan gambaran tentang keadaan elektron yang menempati daerah sekitar inti atom. Penjelasan Bohr tentang atom hidrogen melibatkan kombinasi antara teori klasik Rutherford dan teori kuantum Planck, yang diungkapkan oleh empat postulat, sebagai berikut:
- Hanya ada satu set orbit tertentu yang diperbolehkan untuk satu elektron dalam atom hidrogen. Orbit ini dikenal sebagai keadaan gerak stasioner elektron dan merupakan jalur melingkar di sekitar nukleus.
- Selama elektron berada pada lintasan stasioner, energi elektron tetap konstan sehingga tidak ada energi yang dipancarkan atau diserap dalam bentuk radiasi.
- Elektron hanya dapat berpindah dari satu jalur stasioner ke jalur stasioner lainnya. Dalam transisi ini sejumlah energi terlibat, ukurannya menurut persamaan Planck, ΔE = hv.
- Jalur stasioner yang diperbolehkan memiliki besaran dengan sifat tertentu, terutama yang disebut sifat momentum sudut. Besarnya momentum sudut adalah kelipatan dari h/2μ atau nh/2μ, di mana n adalah bilangan bulat dan h adalah konstanta Planck.
Menurut model atom Bohr, elektron mengorbit inti dalam lintasan tertentu yang disebut kulit elektron atau tingkat energi. Tingkat energi terendah adalah kulit elektron bagian dalam, semakin banyak yang keluar, semakin tinggi jumlah kulitnya dan semakin tinggi tingkat energinya.
Kelemahan:
Model atom ini tidak dapat menjelaskan spektrum warna atom berelektron banyak.
Teori Atom Modern
Model atom mekanika kuantum dikembangkan oleh Erwin Schrodinger (1926). Sebelum Erwin Schrodinger, seorang ahli berkebangsaan Jerman, Werner Heisenberg mengembangkan teori mekanika kuantum yang dikenal dengan prinsip ketidakpastian, yaitu “Tidak mungkin secara akurat mengukur posisi dan momentum suatu benda pada waktu yang sama, yang dapat menentukan probabilitas penemuan elektron pada jarak tertentu dari inti atom.
Wilayah ruang di sekitar inti dengan kemungkinan menangkap elektron disebut orbital. Bentuk dan tingkat energi orbital dirumuskan oleh Erwin Schrodinger Erwin Schrodinger memecahkan persamaan untuk mendapatkan fungsi gelombang untuk menggambarkan kemungkinan batas menemukan elektron dalam tiga dimensi.
Model atom dengan orbital elektron disebut model atom modern atau model atom mekanika kuantum saat ini, seperti yang ditunjukkan pada gambar berikut.
Awan elektron di sekitar nukleus menunjukkan di mana kemungkinan besar elektron berada. Orbital menggambarkan tingkat energi elektron. Orbital dengan tingkat energi yang sama atau hampir sama membentuk subkulit. Beberapa subkulit bergabung membentuk sebuah kulit, sehingga sebuah kulit terdiri dari beberapa subkulit dan sebuah subkulit terdiri dari beberapa orbital. Walaupun posisi cangkangnya sama, namun posisi orbitnya belum tentu sama.
Demikian artikel dari lecturemipa.com tentang Teori Atom: Dalton, Rutherford, Thomson, Bohr, Modern, Development, semoga artikel ini bermanfaat bagi anda semua.
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa