Definisi Reaksi Redoks
Reaksi redoks adalah persamaan kimia di mana bilangan oksidasi atom yang terlibat dalam reaksi kimia berubah ketika reaksi terjadi. Reaksi adalah persamaan kimia di mana bilangan oksidasi atom yang terlibat dalam reaksi kimia berubah ketika reaksi berlangsung. Definisi ini memperkenalkan kita pada konsep fundamental lain yang sangat penting dalam kimia, bilangan oksidasi. Mari kita definisikan.
Bilangan oksidasi adalah bilangan yang persis sama dengan valensi atom, tetapi bilangan oksidasi membawa tanda. Tanda ini mengungkapkan sifat muatan pada spesies yang bersesuaian ketika terbentuk dari atom netral. Mari kita pahami ini melalui sebuah contoh. Bilangan oksidasi klorin dalam asam klorida (HCl) adalah -1, dalam asam klorida (HClO3) adalah +5 dan dalam asam perklorat (HClO4) adalah +7.
Untuk menghitung bilangan oksidasi, kita harus mempertimbangkan keadaan oksidasi yang berbeda dari semua atom dalam molekul dan kemudian menyamakan jumlah semuanya dengan muatan total pada molekul. Ada beberapa aturan untuk menentukan bilangan oksidasi atom dalam suatu molekul. Namun, di sini kita hanya akan melihat bagaimana mencari bilangan oksidasi Cl dalam HClO3.
Contoh Reaksi Redoks
Pembentukan hidrogen fluorida
Reaksi: H2 + F2 = 2HF
Zat teroksidasi: Hidrogen
Debu mengurangi: Fluor
Reaksi oksidasi: H2 → 2H + + 2e –
Reaksi reduksi: F 2 + 2e – → 2F –
Pada reaksi pertama, hidrogen teroksidasi dengan menaikkan bilangan oksidasi dari 0 menjadi 1, sedangkan pada reaksi kedua, fluor berkurang dengan menurunkan bilangan oksidasi dari 0 menjadi -1. Akhirnya, muatan total pada molekul yang terbentuk adalah nol karena jumlah elektron yang diperoleh selama oksidasi dikonsumsi selama proses reduksi. Akhirnya, persamaan menjadi,
H2 → 2H+ + 2e – + F2 + 2e- → 2F – = H2+ F2= 2H + + 2F –
H2 + H2 → 2H+ + 2F – → 2HF
Beberapa contoh lagi
Beberapa contoh telah disebutkan di sini. Dalam contoh ini, hanya reaksi lengkap yang disebutkan, bukan reaksi setengah sel.
Reaksi antara larutan Fe(II) dan CuSO4: Fe + CuSO4 + → FeSO4 + Cu (Fe teroksidasi, Cu tereduksi)
Oksidasi Fe(II) menjadi Fe(III) oleh hidrogen peroksida dan asam: 2 Fe2+ + H2O2 + 2 H + → 2 Fe3+ + 2 H2O
Oksidasi glukosa menjadi karbon dioksida: C6 H12 O 6 + 6 O2 → 6 CO 2 + 6 H2O
Reaksi antara Kalium Permanganat dan Natrium Sulfit: 2 KMnO4 + 3 Na 2 SO 3 + H 2 O → 2 MnO 2 + 3 Na 2 SO 4 + 2 KOH
Reaksi asam dan basa: 3 CU + 8 HNO3 → 3 CuSO 4 + 8 NO (g) + 4 H 2 O
Konsep reaksi redoks
-
Konsep reaksi redoks berdasarkan kombinasi dan pelepasan oksigen
Pada awal sekitar abad ke-18, konsep reaksi oksidasi dan reduksi didasarkan pada penggabungan unsur/senyawa dengan oksigen membentuk oksida, dan pelepasan oksigen dari senyawa. Reaksi oksidasi adalah reaksi yang menggabungkan oksigen dengan unsur atau senyawa seperti pada contoh berikut:
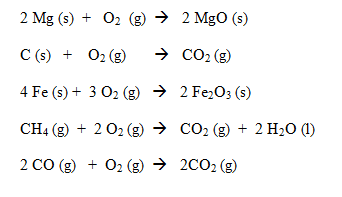
Reaksi reduksi adalah reaksi yang melepaskan oksigen dari senyawanya, seperti pada contoh berikut:
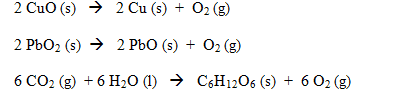
-
Konsep reaksi redoks berdasarkan keuntungan dan kerugian elektron
Pada pergantian abad ke-20, para ahli melihat sifat dasar reaksi oksidasi dan reduksi dalam kaitannya dengan ikatan kimianya, yaitu transfer elektron. Reaksi oksidasi melibatkan pelepasan elektron, sedangkan reaksi reduksi melibatkan perolehan elektron. Konsep ini dapat diterapkan pada reaksi yang tidak melibatkan oksigen.
Reaksi oksidasi adalah reaksi yang melepaskan elektron, sedangkan reaksi reduksi adalah reaksi yang menerima elektron. Dilihat dari transfer elektron, reaksi oksidasi dan reduksi selalu terjadi bersamaan. Artinya, ada zat yang kehilangan elektron atau mengalami oksidasi dan ada zat yang menerima elektron atau mengalami reduksi. Reaksi berikut menunjukkan transfer elektron.
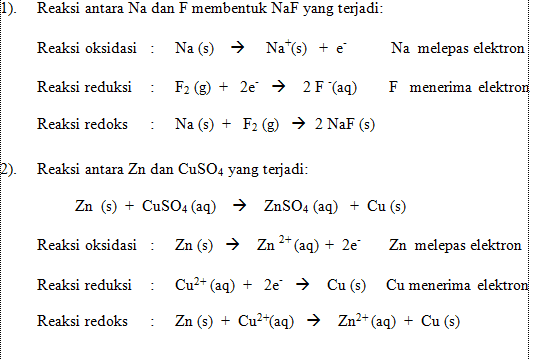
Bilangan oksidasi
Untuk menerapkan konsep reaksi oksidasi dan reduksi berdasarkan perubahan bilangan oksidasi, terlebih dahulu harus diketahui apa itu bilangan oksidasi dan bagaimana menentukan nilai bilangan oksidasi suatu unsur. Bilangan oksidasi suatu atom suatu unsur adalah muatan yang dimiliki atom tersebut. Jika elektron valensi cenderung tertarik ke atom lain yang berasosiasi dengannya, elektronegatifitasnya akan relatif lebih besar.
Secara umum, aturan tersebut berlaku untuk 2 atom yang berikatan (ionik atau kovalen):
- Atom unsur dengan keelektronegatifan lebih rendah memiliki bilangan oksidasi positif.
- Atom unsur dengan keelektronegatifan lebih besar memiliki bilangan oksidasi negatif.
Untuk menentukan bilangan oksidasi atom suatu unsur, aturan berikut berlaku:
- Bilangan oksidasi atom dalam unsur bebas sama dengan 0 (nol).
Contoh:
Bilangan oksidasi atom pada unsur Na, Fe, C, H2kl2P4dll.8 sama dengan 0 (nol).
- Bilangan oksidasi ion monoatomik sama dengan muatan ion.
laporan bilangan oksidasi
Membedakan konsep oksidasi-reduksi ditinjau dari kombinasi dan pelepasan oksigen, pelepasan dan penerimaan elektron, serta kenaikan dan penurunan bilangan oksidasi
Menentukan bilangan oksidasi atom/unsur dalam senyawa atau ion
Reaksi redoks mengandung dua pengertian, yaitu reaksi reduksi dan reaksi oksidasi. Pengertian reaksi oksidasi dan reaksi reduksi berkembang sejalan dengan perkembangan ilmu kimia.
Perkembangan Reaksi Redoks
Pada oksidasi pertama merupakan reaksi yang mengikat oksigen melalui suatu zat.
Contoh
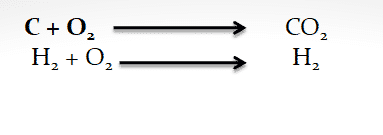
Reduksi adalah reaksi pelepasan oksigen oleh suatu zat
Contoh:
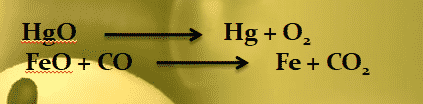
Karena reaksi kimia tidak hanya melibatkan oksigen. Misalnya reaksi antara gas klorin dan natrium.
Panjang reaksi redoks
Redoks adalah istilah yang menjelaskan perubahan bilangan oksidasi (keadaan oksidasi) atom dalam reaksi kimia.
Ini dapat berupa proses redoks sederhana seperti oksidasi karbon untuk menghasilkan karbon dioksida, atau reduksi karbon oleh hidrogen untuk menghasilkan metana (CH4), atau dapat berupa proses kompleks seperti oksidasi gula dalam tubuh manusia oleh urutan transfer elektron yang rumit.
Istilah redoks berasal dari dua konsep, yaitu reduksi dan oksidasi. Ini dapat dengan mudah dijelaskan sebagai berikut:
- Oksidasi menggambarkan hilangnya elektron oleh molekul, atom atau ion
- Reduksi menggambarkan perolehan elektron oleh molekul, atom, atau ion.
Meskipun sangat cocok untuk digunakan dalam berbagai keperluan, namun penjelasan di atas kurang tepat. Oksidasi dan reduksi mengacu pada perubahan bilangan oksidasi karena transfer elektron yang sebenarnya tidak akan selalu terjadi. Jadi oksidasi lebih baik didefinisikan sebagai peningkatan bilangan oksidasi, dan reduksi sebagai penurunan bilangan oksidasi. Dalam prakteknya, transfer elektron akan selalu mengubah bilangan oksidasi, tetapi ada banyak reaksi yang diklasifikasikan sebagai “redoks” meskipun tidak ada transfer elektron dalam reaksi tersebut (misalnya yang melibatkan ikatan kovalen).
Demikian artikel Duniadunia.co.id mengenai Persamaan Reaksi Redoks : Contoh, Konsep, Bilangan, Definisi, Perkembangan, Laporan, Panjang, semoga artikel ini bermanfaat untuk sobat semua.
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa