
Hitte: definisie, verplasing, kapasiteit, tipes, formules en volledige voorbeeldprobleme – Kalorieë is ‘n energie wat maklik aanvaar en maklik vrygestel word sodat dit die temperatuur van die stof kan verander om te styg of daal. Hitte kan ook van een stof na ‘n ander beweeg deur ‘n medium of tussengangers. Byvoorbeeld, twee stowwe wat verskillende temperature het, word in ‘n houer gemeng. Dan sal die temperatuur van die twee voorwerpe dieselfde wees.
Swart se beginsel is ‘n fisiese postulaat rakende hitte wat deur ‘n Skotse wetenskaplike voorgehou is. Die naam van hierdie wet is geneem uit die naam van ‘n Britse wetenskaplike ter waardering van sy dienste, nl. Josef Swart. Spesifieke hitte is ‘n eienskap van ‘n stof wat die hoeveelheid hitte aandui wat nodig is om die temperatuur van ‘n 1 kg stof met 1°C of 1 K te verhoog. Hitte is ‘n vorm van energie. Daar is drie maniere van hitte-oordrag, naamlik geleiding, konveksie en straling.
In die alledaagse lewe gebruik ons dikwels gereedskap gemaak van papier, plastiek, rubber, was, hout, aluminium en selfs materiale wat van yster en staal gemaak is. Sommige voorwerpe is geleiers en sommige is isoleerders.
Lees ook artikels wat verband hou: Termodinamika: Wette van termodinamika 1 2 3 Definisie, beginsels, stelsels, formules en voorbeelde van volledige vrae

Definisie van Calor
Hitte is ‘n energie wat maklik ontvang en maklik vrygestel word sodat dit die temperatuur van die stof kan verander om te styg of daal. Hitte kan ook van een stof na ‘n ander deur ‘n medium of tussenganger beweeg. Dit blyk dat Hitte ‘n vorm van energie is wat nie gesien of gesien kan word nie. En dit blyk dat hitte-energie ook in ander vorme van energie omskep kan word, soos lig, beweging, elektrisiteit, chemie en ander.
Byvoorbeeld, twee stowwe wat verskillende temperature het, word in ‘n houer gemeng. Dan sal die temperatuur van die twee voorwerpe dieselfde wees. Die finale temperatuur is tussen die aanvanklike temperature van die twee stowwe. In hierdie verskynsel beweeg hitte van ‘n hoë temperatuur na ‘n laer temperatuur totdat dit ‘n ewewigstemperatuur bereik.
In 1850, vir die eerste keer Joule met behulp van ‘n werktuig waarin daar vragte is wat val en ‘n groep roerders in ‘n geslote houer water draai. In een siklus doen die vallende vragte ‘n bietjie werk op die water met ‘n massa water m en die water het ‘n temperatuurverhoging van Dt . Hierdie eksperiment verduidelik die teenwoordigheid van energie wat veroorsaak dat hitte in die siklus ontstaan.
- Hitte kan gedefinieer word as die proses om energie van een stof na ‘n ander oor te dra ander met veranderinge in temperatuur.
Lees ook artikels wat verband hou: Ohm se wetteorie: definisie, klank en volledige formules en probleemvoorbeelde
Basiese Swart
Swart se beginsel is ‘n fisiese postulaat rakende hitte wat deur ‘n Skotse wetenskaplike voorgehou is.
Hitte is energie wat oorgedra word van voorwerpe wat ‘n hoë temperatuur het na voorwerpe wat ‘n laer temperatuur het sodat die meting van hitte altyd verband hou met die oordrag van energie. Energie word bewaar sodat voorwerpe wat ‘n hoër temperatuur het, soveel energie sal vrystel VL en voorwerpe wat ‘n laer temperatuur het, sal soveel energie ontvang VT met dieselfde grootte.
Wiskundig word hittemeting dikwels gedoen om die spesifieke hitte van ‘n stof te bepaal. As die spesifieke hitte van ‘n stof bekend is, kan die hitte wat geabsorbeer of vrygestel word bepaal word deur die verandering in temperatuur van die stof te meet. Wanneer jy hierdie vergelyking gebruik, hou in gedagte dat ‘n toename in temperatuur beteken dat die stof hitte ontvang, en ‘n temperatuurdaling beteken dat die stof hitte vrystel.
Kalorimeter is ‘n instrument wat gebruik word om hitte te meet. ‘n Vorm van kalorimeter, hierdie kalorimeter bestaan uit ‘n metaalvat met ‘n bekende spesifieke hitte. Hierdie houer word gewoonlik in ‘n ander houer geplaas wat ietwat groter is. Die twee vate word geskei deur ‘n isolerende materiaal, soos kurk of wol. Die gebruik van die buitenste houer is as ‘n beskermer sodat hitte-uitruiling met die omgewing rondom die kalorimeter verminder kan word.
Die kalorimeter is ook toegerus met ‘n roerstaaf. Wanneer stowwe in die kalorimeter gemeng word, moet die water in die kalorimeter geroer word sodat ‘n egalige temperatuur verkry word deur twee stowwe met verskillende temperature te meng. Die roerstaaf is gewoonlik van dieselfde materiaal as die kalorimetervat gemaak.
‘n Stof waarvan die spesifieke hitte bekend is, word tot ‘n sekere temperatuur verhit. Dan word die stof in die kalorimeter geplaas wat gevul is met water met ‘n bekende temperatuur en massa. Vervolgens word die kalorimeter geroer totdat die temperatuur konstant bly.
Lees ook artikels wat verband hou: Elektromagnetiese golwe: definisie, eienskappe, tipes en formules saam met volledige probleemvoorbeelde
Spesifieke hitte
Spesifieke hitte is ‘n eienskap van ‘n stof wat die hoeveelheid hitte toon wat nodig is om die temperatuur van ‘n stof met ‘n massa van 1 kg met 1°C of 1 K te verhoog. By dieselfde temperatuur blyk dit dat elke voorwerp hitte sal absorbeer energie met ‘n ander hoeveelheid. Daar is byvoorbeeld vier balle wat elk van aluminium, yster, koper en blik gemaak is. Hierdie vier balle het dieselfde massa en word in ‘n houer gevul met kookwater geplaas.
Na 30 minute sal die vier balle termiese ewewig met die water bereik en dieselfde temperatuur as die water hê. Daarna is die vier balletjies verwyder en bo-op die paraffien geplaas. Die aluminiumballetjies kan die paraffien smelt en deur die paraffien val. ’n Paar sekondes later het die ysterbal dieselfde ervaar.
Koperballetjies kan paraffien net gedeeltelik smelt, terwyl loodballetjies skaars paraffien kan smelt. Die vier balletjies absorbeer hitte uit die kookwater en dra dan die hitte oor na die paraffien sodat die paraffien smelt.
Omdat elke voorwerp ‘n ander vermoë het om paraffien te smelt, sal elke bal hitte teen ‘n ander tempo van die water na die paraffien oordra. Die vermoë wat elk van hierdie voorwerpe besit, hou verband met die spesifieke hitte van die voorwerp. Die spesifieke hitte van ‘n voorwerp kan gedefinieer word as die hoeveelheid hitte wat nodig is om te verhoog temperatuur van 1 kg van ‘n stof by 1K.
Spesifieke hitte dui op die vermoë van ‘n voorwerp om hitte te absorbeer. Hoe groter die spesifieke hitte van ‘n voorwerp, hoe groter is die voorwerp se vermoë om hitte te absorbeer.
Kalorieë eenheid
Die eenheid van hitte is die joule (J) wat geneem is van die naam van ‘n wetenskaplike wat bygedra het tot die veld van fisika, nl. James Joule. Nog ‘n eenheid van hitte is die kalorie. Die verhouding tussen die eenheid joule en kalorieë, naamlik 1 kalorie = 4,184 joule.
Stoom hitte
Damphitte is die hoeveelheid hitte per massa-eenheid wat aan ‘n stof by sy kookpunt gegee word sodat die vloeibare toestand heeltemal verander na ‘n gasvormige toestand by daardie kookpunt.
Verdamping
Verdamping is die gebeurtenis waar ‘n stof van ‘n vloeistof in ‘n gasvormige stof verander word. Verdamping in vloeistof vind plaas omdat daar hitte ontvang word. Byvoorbeeld, water wat aanhoudend verhit word, sal verdamp om in waterdamp te verander wat ‘n gas is. Die volgende is verskeie maniere om die verdampingsproses te bespoedig:
- verhoging van die temperatuur (verhitting) van vloeistowwe,
- vergroot die oppervlak van die vloeistof
- vloei van lug oor die oppervlak van die vloeistof,
- verminder die druk bo die oppervlak van die vloeistof.
Temperatuurverandering
Die verandering in temperatuur is die verskil tussen die finale temperatuur en die aanvanklike temperatuur van ‘n stof wat na ‘n tyd bereken moet word. Veranderinge in temperatuur vind plaas as gevolg van hitte wat vrygestel of geabsorbeer word uit of in die omgewing waar die stof geleë is.
Hitte-oordrag
Soos ons vroeër verduidelik het, vind hitte-oordrag plaas vanaf voorwerpe met hoë temperatuur na voorwerpe met lae temperatuur. Daar is drie tipes hitte-oordrag wat kan plaasvind, naamlik soos volg:
1. Geleiding Hitte-oordrag
Hitte-oordrag deur geleiding is ‘n oordrag van hitte deur ‘n tussenstof (metaal) sonder dat dit gepaard gaan met die permanente oordrag van die deeltjies van daardie stof. Byvoorbeeld, wanneer ons die een kant van die metaal verhit, sal die ander kant van die metaal ook verhit omdat hitte-oordrag van hoë temperatuur na lae temperatuur plaasvind.
Wanneer die een kant van die metaal verhit word, sal die deeltjies in die metaalpunt vibreer en ‘n vibrasie laat voorkom in ander deeltjies wat daaraan gekoppel is. Sodat al die metaaldeeltjies sal vibreer al word net een kant van die metaal verhit, is dit nou wat hitte-oordrag sal stimuleer.
2. Hitte-oordrag deur konveksie
Hitte-oordrag deur konveksie is ‘n oordrag van hitte deur ‘n stof wat gepaard gaan met die beweging van dele van die stof. Konveksie kan in vloeistowwe of gasse voorkom. Daar is twee tipes hitte-oordrag deur konveksie, naamlik soos volg:
- Natuurlike konveksie naamlik ‘n tipe konveksie wat deur dryfkrag sonder eksterne faktore beïnvloed word, en veroorsaak word deur verskille in die digtheid van voorwerpe. Byvoorbeeld, wanneer water verhit word, styg die digtheid van warmwaterdeeltjies weg van die vuur en word dit deur ander waterdeeltjies met ’n laer temperatuur vervang. Hierdie proses maak dat al die vloeistofdeeltjies perfek warm sal wees.
- Geforseerde konveksie naamlik een tipe konveksie wat plaasvind as gevolg van die invloed van eksterne faktore (bv. druk), en hitte-oordrag word doelbewus / gedwonge uitgevoer. Dit beteken dat die hittevloei gedwing word om te gaan waarheen jy wil gaan met behulp van eksterne faktore soos druk. ‘n Voorbeeld is ‘n waaier wat koue lug na ‘n warm plek sal bring, en ‘n motorverkoeler wat ‘n enjinverkoelingstelsel het.
3. Stralingshitte-oordrag
Stralingshitte-oordrag is ‘n hitte-oordragproses wat nie ‘n tussenstof gebruik nie. Stralingshitte-oordrag verskil van geleiding en konveksie. In bestraling, vir hitte-oordrag om plaas te vind, hoef die twee voorwerpe nie aan te raak nie, want hitte kan beweeg sonder ‘n tussenliggende stof. Dit beteken dat die hitte in alle rigtings deur die hittebron vrygestel sal word, en in alle rigtings sal vloei. ‘n Voorbeeld is wanneer ons vanuit enige hoek naby ‘n vreugdevuur is, sal ons steeds die warmte van die bron van die vuur voel.
4. Voorkoming van hitte-oordrag
Hitte-oordrag deur geleiding, konveksie en bestraling kan voorkom word deur die kamer te isoleer. ‘n Voorbeeld is die eenvoudige toepassing van hierdie metode, naamlik op ‘n termosfles. Die termosfles word gebruik om die watertemperatuur warm te hou deur hitte-oordrag te voorkom.
Hitte kapasiteit
Op grond van die navorsing is gevind dat indien hitte op twee verskillende voorwerpe toegepas word, dit verskillende temperature sal produseer.Byvoorbeeld, wanneer olie en water tot dieselfde temperatuur verhit word, sal olie ‘n temperatuurverandering hê wat 2 keer groter is as water. Dit is as gevolg van die verskil in die spesifieke hitte wat ‘n voorwerp het.
Spesifieke hitte van ‘n voorwerp is die hoeveelheid hitte wat benodig word om die temperatuur van 1 kg van die voorwerp se massa tot 1 graad Celsius te verhoog. Die eenheid van Spesifieke Hitte is Kalorie / GramoCelcius of in die Internasionale Stelsel word dit bepaal deur Joule / KilogramoCelcius. Spesifieke hitte kan in die volgende vergelyking geskryf word: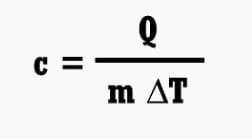
Inligting:
Q = Hitte (J)
m : Voorwerpmassa (kg)
c = Spesifieke hitte (J Kg oC)
ΔT = Temperatuurverandering (oC)
Daarbenewens is daar nog ‘n formule vir die bepaling van die hittekapasiteit self, naamlik: C = m. c
Inligting:
- C = hittekapasiteit (J/K)
- m = massa van voorwerpe wat hitte ontvang of vrystel (kg)
- c = spesifieke hitte van stof (J/kg.K)
Intussen is die hittekapasiteit die hoeveelheid hitte wat benodig word om die temperatuur van die stof met 1 graad Celsius te verhoog. As die hitte Q ‘n temperatuur van t produseer, kan die hittekapasiteit geformuleer word: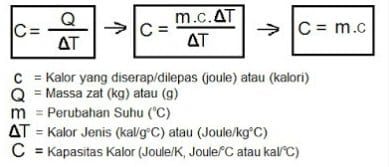
Voorbeelde van kalorie-vrae
‘n Stuk koper het ‘n massa van 5 kg en ‘n temperatuur van 20°C. As die spesifieke hitte van koper 390J/kg°C is. Hoeveel hitte word benodig om koper tot 100°C te verhit?
Voltooiing:
m = 5 kg
c = 390 J/kg°C
∆T = T2-T1
= 100-20 = 80°C
Q = m • c • ∆T
= 5-390-80 J
= 156 000 J = 156 kJ
Dit is die volledige resensie,Hopelik is dit wat hierbo nagegaan is nuttig vir lesers. Dit is al en dankie.
Lees ook ander verwante verwysingsartikels hier:
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa


