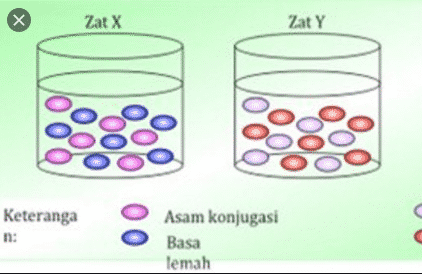
Solusi penyangga, larutan penyanggaatau buffer adalah larutan yang digunakan untuk mempertahankan nilai pH tertentu agar tidak banyak berubah selama reaksi kimia. Ciri khas larutan penyangga ini adalah perubahan pH hanya sedikit dengan penambahan sedikit asam kuat atau basa kuat.
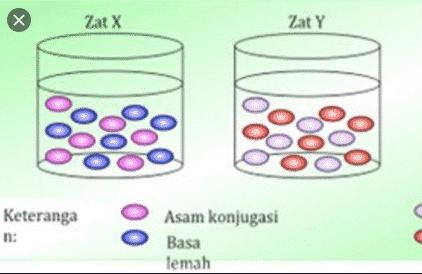
Larutan penyangga terdiri dari asam lemah dan basa konjugatnya atau basa lemah dan asam konjugatnya. Reaksi antara kedua komponen ini dikenal sebagai reaksi asam-basa konjugat.
Komponen larutan penyangga
Secara umum, larutan penyangga digambarkan sebagai campuran yang terdiri dari:
- Asam lemah (HA) dan basa konjugatnya (ion A-), campuran ini menghasilkan larutan asam.
- Basa lemah (B) dan asam konjugatnya (BH+), campuran ini menghasilkan larutan basa.
Komponen larutan buffer dibagi menjadi:
-
Larutan penyangga asam
Larutan ini mempertahankan pH dalam kisaran asam (pH <7). Untuk mendapatkan larutan ini dapat dibuat dari asam lemah dan garamnya yang merupakan basa konjugat dari asam tersebut. Cara lainnya adalah dengan mencampurkan asam lemah dengan basa kuat dimana asam lemah dicampur secara berlebihan. Campuran tersebut akan menghasilkan garam yang mengandung basa konjugasi dari asam lemah yang dimaksud. Umumnya digunakan basa kuat seperti Natrium Na), Kalium, Barium, Kalsium dan lain-lain.
-
Larutan penyangga basa
Larutan ini mempertahankan pH dalam kisaran basa (pH > 7). Larutan ini dapat dibuat dari basa lemah dan garam, yang garamnya berasal dari asam kuat. Cara lain adalah dengan mencampurkan basa lemah dengan asam kuat dimana basa lemah dicampur secara berlebihan.
Bagaimana solusi buffer bekerja
Larutan buffer mengandung komponen asam dan basa dengan asam dan basa konjugatnya, sehingga dapat mengikat ion H+ dan ion OH-. Sehingga penambahan sedikit asam kuat atau basa kuat tidak mengubah pH secara signifikan. Inilah cara kerja solusi buffer:
Cara kerjanya dapat dilihat pada larutan buffer yang mengandung CH3COOH dan CH3COO- yang berada dalam kesetimbangan. Dengan proses sebagai berikut:
Penambahan asam (H+) akan menggeser kesetimbangan ke kiri. Dimana ion H+ yang ditambahkan akan bereaksi dengan ion CH3COO- membentuk molekul CH3COOH.
CH3COO-(aq) + H+(aq) → CH3COOH(aq)
Saat menambahkan basis
Jika yang ditambahkan adalah basa, maka ion OH basa tersebut akan bereaksi dengan ion H+ membentuk air. Hal ini akan menyebabkan kesetimbangan bergeser ke kanan sehingga konsentrasi ion H+ dapat dipertahankan. Jadi, penambahan basa menyebabkan penurunan komponen asam (CH3COOH), bukan ion H+. Basa yang ditambahkan bereaksi dengan asam CH3COOH membentuk ion CH3COO- dan air.
CH3COOH(aq) + OH-(aq) → CH3COO-(aq) + H2O(l)
Cara kerjanya dapat dilihat pada larutan penyangga yang mengandung NH3 dan NH4+ yang berada dalam kesetimbangan. Dengan proses sebagai berikut:
Jika asam ditambahkan, ion H+ dari asam akan berikatan dengan ion OH-. Hal ini menyebabkan kesetimbangan bergeser ke kanan, sehingga konsentrasi ion OH dapat dipertahankan. Selain itu, penambahan ini menyebabkan pengurangan komponen dasar (NH3), bukan ion OH. Asam yang ditambahkan bereaksi dengan basa NH3 membentuk ion NH4+.
NH3 (aq) + H+(aq) → NH4+ (aq)
Jika basa ditambahkan, kesetimbangan bergeser ke kiri, sehingga konsentrasi ion OH- dapat dipertahankan. Basa yang ditambahkan bereaksi dengan komponen asam (NH4+), membentuk komponen basa (NH3) dan air.
NH4+ (aq) + OH-(aq) → NH3 (aq) + H2O(l)
Perhitungan pH larutan penyangga
Konstanta ionisasi dapat digunakan untuk menentukan konsentrasi ion H+ dalam larutan dengan rumus berikut:
[H+] = Ka xa/valxg
atau
pH = p Ka – log a/g
dengan, Ka = tetapan ionisasi asam lemah
a = jumlah mol asam lemah
g = jumlah mol basa konjugasi
Konstanta ionisasi dapat digunakan untuk menentukan konsentrasi ion H+ dalam larutan dengan rumus berikut:
[OH-] = Kbxb/valxg
atau
pH = p Kb – log b/g
dengan, Kb = tetapan ionisasi basa lemah
b = jumlah mol basa lemah
g = jumlah mol asam terkonjugasi
Fungsi Resolusi Penyangga
Keberadaan larutan penyangga ini dapat kita lihat dalam kehidupan sehari-hari, seperti dalam dunia kedokteran, fotografi, industri kulit dan pewarna. Selain aplikasi tersebut, terdapat fungsi penerapan konsep larutan buffer ini pada tubuh manusia seperti pada cairan tubuh. Cairan tubuh ini dapat berupa cairan intraseluler atau cairan ekstraseluler.
Dimana sistem buffer utama pada cairan intraseluler seperti H2PO4- dan HPO42- yang dapat bereaksi dengan asam dan basa. Sedangkan untuk sistem buffer dapat menjaga pH darah hampir konstan yaitu sekitar 7,4. Selain itu, penerapan larutan penyangga ini dapat kita jumpai dalam kehidupan sehari-hari, seperti pada obat tetes mata. Tetes mata memiliki pH yang sama dengan cairan tubuh kita, sehingga tidak menimbulkan efek samping.
Demikian artikel Duniaduniadik.co.id tentang larutan buffer: pengertian, komponen, cara kerja, perhitungan, rumus, fungsi, semoga artikel ini bermanfaat untuk sobat semua.
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa


